Étude Caplavie
Écrit par cnr-mat
Objectifs de l’étude
Objectif principal
Évaluer l'effet de la stratégie caplacizumab + EP + RTX au cours du PTT à la phase aiguë sur la mortalité à 30 jours.
Objectifs secondaires
Évaluer l'effet de la stratégie caplacizumab + EP + RTX sur :
- la mortalité précoce (J15) ;
- la fréquence de rémission complète, d’exacerbation et de PTT réfractaires au décours de l’épisode ;
- le délai de normalisation des plaquettes ;
- le pourcentage de normalisation des plaquettes à J30 ;
- les séquelles neuro-cognitives et la qualité de vie.
Méthodes
Étude prospective multicentrique
Inclusion
Centres composant le CNR-MAT.
Calendrier
- Durée d’observation du patient : 3 mois
- Durée de l’étude : 27 mois
Calcul d’effectifs
- Le plan d’analyse statistique suivra la méthode en deux étapes de Fleming correspondant à une étude de phase 2 non comparative où il s’agit de comparer la proportion observée d’un événement (décès, rechute …) sur les données de l’étude à la proportion de référence ;
- mortalité de référence à J30 de 15%, mortalité escomptée à J30 de 6% ;
- risque de première espèce de 2,5% en formulation unilatérale ;
- puissance statistique de 80% ;
- inclusion de 51 patients à la première étape : si le nombre de décès est d’au moins 6, l’étude est arrêtée pour futilité. Si le nombre de décès est d’au plus 2, l’étude est arrêtée pour efficacité ;
- si le nombre de décès est compris entre 3 et 5 lors de la première étape, l’essai continue et 54 patients supplémentaires sont recrutés à la seconde étape, soit un total de 105 patients en tout si le nombre de décès total est inférieur ou égal à 8 sur 105, l’étude conclut à l’efficacité, alors qu’elle conclura à la non mise en évidence de l’efficacité dans le cas contraire.
Schéma de l'étude
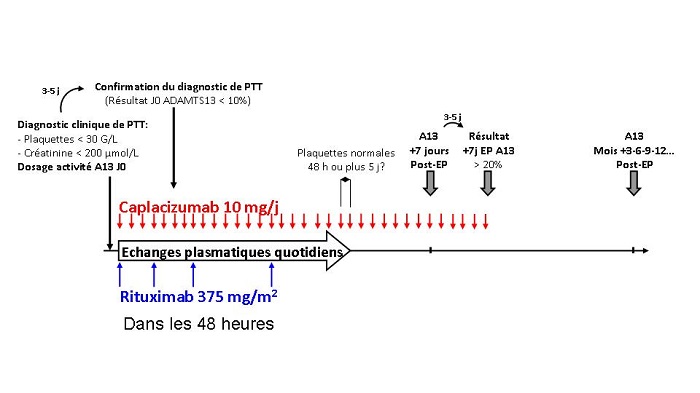
Questions soulevées
« Encadrement » de l’utilisation d’une nouvelle molécule avec comme seule intervention le dosage plus précoce d’ADAMTS13 pour guider la poursuite (activité ADAMTS13 < 20%) ou l’arrêt (activité ADAMTS13 ≥ 20%) du traitement par caplacizumab.
Intérêts
- Réduction de la durée et donc du coût ; à n’envisager qu’une fois le remboursement obtenu (actuellement utiliser le CAPLA conformément au libellé de l’ATU) ;
- homogénéiser son utilisation et maintenir des surveillances d’ADAMTS13 dans l’idée d’une première étude de registre « rétro/prospective ».
L’étude entre dans le cadre du soin courant (l’utilisation du rituximab d’emblée devrait maintenant être considérée comme faisant partie du soin courant [P. Coppo, A. Cuker, JN George. Res Pract Thromb Haemost 2018]).
Dernières actualités
- PTT congénital : La protéine ADAMTS13 recombinante bientôt disponible en accès précoce - publié le 26/03/24, [13261 clics]
- Essais thérapeutiques en cours - publié le 12/02/24, [12845 clics]
- Journée AD'venir 2023 - publié le 31/01/24, [11438 clics]
- Relabellisation du CNR-MAT - publié le 10/01/24, [43676 clics]
- Réunion du Centre de Référence 2023 - publié le 01/02/23, [14767 clics]













