La Clinique
Les microangiopathies thrombotiques (MAT) représentent un ensemble de maladies caractérisées par l’association d’une anémie par fragmentation des globules rouges, une baisse du taux de plaquettes (thrombopénie), et une souffrance d’un ou plusieurs organes. Les MAT sont en règle des maladies graves, mais diagnostiquées rapidement et traitées correctement, leur pronostic peut être excellent. Elles sont liées à la formation de multiples petits caillots dans les petits vaisseaux de nombreux organes, entraînant la souffrance de ces organes. Ces maladies peuvent toucher des personnes de tout âge, bien que certaines formes soient plus fréquemment observées chez l’enfant, alors que d’autres sont plus volontiers rencontrées chez l’adulte. Ces maladies ne sont pas contagieuses. Elles touchent des individus partout dans le monde.
Il existe plusieurs types de MAT. Celles-ci doivent être distingués les unes des autres car leur traitement et leur pronostic peut varier.
Écrit par cnr-mat
le 24 Mars 2024
Un traitement imparfait
Le PTT congénital se caractérise par des poussées de la maladie tout au long de la vie, typiquement déclenchées par des épisodes infectieux. La thrombopénie, ainsi que l’anémie hémolytique sont intermittentes ou parfois permanentes. Dans tous les cas, la formation de micro-thrombi dans différents organes expose les patients à des complications graves à court et à long terme (accidents vasculaires cérébraux ischémiques, infarctus du myocarde, douleurs abdominales, insuffisance rénale, etc…). Le traitement actuel repose sur l’administration de plasma thérapeutique toutes les semaines à tous les quinze jours. Cependant ce traitement permet un contrôle souvent incomplet de la maladie, et s’associe à des effets secondaires ; de plus, il nécessite des hospitalisations régulières, impactant la qualité de vie.
Mis à jour le 27 Mars 2024
Écrit par Elise
le 17 Janvier 2018
Document
Introduction
Une nouvelle importante en 2017 dans le domaine du PTT autoimmun est la communication officielle des résultats de l’essai thérapeutique à promotion industrielle HERCULES, qui est positif. Ces résultats, qui confirment ceux de l’étude précédente TITAN, ont été présentés au dernier congrès de la Société Américaine d’Hématologie (décembre 2017) à la session des Late Breaking Abstracts.
Le schéma de l’étude était le suivant :
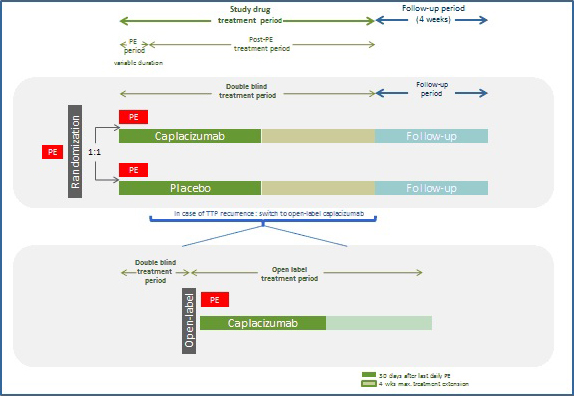
Des patients traités pour un épisode aigu de PTT et ayant bénéficié d’un premier échange plasmatique (EP) ont été randomisés avec un ratio 1:1 entre un bras placebo et un bras caplacizumab (CAPLA), en plus d’EP quotidiens et d’une corticothérapie (traitement standard). La période de traitement couvrait la durée des EP quotidiens et les 30j suivant leur arrêt. A la fin de cette période , une extension de traitement hebdomadaire sur un maximum de 4 semaines pouvait être proposée en cas d’un déficit sévère persistant en ADAMTS13, en plus de l’optimisation du traitement immunosuppresseur. Les patients ont été suivis 28 jours après la dernière administration du produit à l’étude.
Lire la suite...
Mis à jour le 16 Février 2022
Écrit par cnr-mat
le 29 Novembre 2011
Informations médicales :
Vincristine [Médicaments immunosuppresseurs]
Nom alternatif : oncovin
Commentaire
La vincristine n’est quasiment plus utilisée dans le PTT autoimmun. En effet, les cas de PTT réfractaires ou sujets à des exacerbations multiples sont devenus exceptionnels à l’ère de l’utilisation systématique du caplacizumab et du rituximab. Historiquement, des cas cliniques ou des études rétrospectives ont rapporté l’efficacité de la vincristine dans les années 1990 (Welborn, Emrick et al. 1990; O'Connor, Bruce-Jones et al. 1992; Bobbio-Pallavicini, Porta et al. 1994). Certains auteurs ont également utilisé la vincristine en association aux échanges plasmatiques dès le début de la prise en charge (Mazzel, Pepkowitz et al. 1998), avec dans une étude portant sur 12 patients une rémission durable chez tous le patients (Ziman, Mitri et al. 2005). Cependant, une telle utilisation s’est associée à des cas de neuropathie toxique.
Mis à jour le 13 Février 2022
Écrit par cnr-mat
le 13 Février 2022
Informations médicales :
Caplacizumab [Antithrombotique ]
Nom alternatif : Cablivi
Utilisation
Le traitement par caplacizumab, en association aux échanges plasmatiques et au traitement immunosuppresseur par corticoïdes/rituximab dès le diagnostic de PTT autoimmun, permet de réduire le temps de normalisation plaquettaire. Il permet également une réduction significative des décès liés au PTT, des exacerbations de PTT ou des évènements thromboemboliques majeurs sous traitement. Cette thérapeutique a un profil de tolérance favorable avec des saignements muco-cutanés rapportés comme étant l’évènement indésirable le plus fréquent. Le caplacizumab, grâce à l’inhibition rapide de l’adhésion des plaquettes au facteur Willebrand, représente une nouvelle modalité thérapeutique dans la prise en charge du PTT autoimmun. L’association EP + rituximab/corticoïdes + Caplacizumab représente ainsi un nouveau standard thérapeutique. Il est recommandé de poursuivre le traitement par caplacizumab jusqu’à ce que l’activité ADAMTS13 atteigne un seuil protecteur, estimé à 20% (ce qui traduit l’efficacité du traitement immunomodulateur), afin de protéger les malades des exacerbations et des rechutes précoces (voir Caplacizumab Treatment for Acquired Thrombotic Thrombocytopenic Purpura ; A regimen with caplacizumab, immunosuppression and plasma exchange prevents unfavorable outcomes in immune-mediated TTP).
Mis à jour le 13 Février 2022
Écrit par cnr-mat
le 29 Novembre 2011
Utilisation
Le rituximab est désormais prescrit dès le diagnostic de PTT autoimmun chez tous les patients (voir ISTH guidelines for treatment of thrombotic thrombocytopenic purpura). Il permet de raccourcir la durée de traitement par échanges plasmatiques, mais surtout par caplacizumab. L’association systématique du rituximab au traitement par échanges plasmatiques, corticoïdes et caplacizumab permet d’atteindre un seuil d’activité ADAMTS13 protecteur (20%) chez 50% des patients à J28 du dernier échange plasmatique. Cependant, 10% des patients vont conserver un déficit sévère en ADAMTS13 (activité <10%) au-delà de J56, ce qui peut justifier de renforcer le traitement immunosuppresseur (voir A regimen with caplacizumab, immunosuppression and plasma exchange prevents unfavorable outcomes in immune-mediated TTP).
L’utilisation maintenant systématique du rituximab dès le diagnostic de PTT autoimmun permet également de prévenir les rechutes précoces. Chez les patients en rémission clinique et qui développent durant le suivi un déficit sévère en ADAMTS13, un traitement préemptif par rituximab permet de normaliser l’activité ADAMTS13 dans la grande majorité des cas, protégeant les patients d’une rechute clinique (voir Preemptive rituximab infusions after remission efficiently prevent relapses in acquired thrombotic thrombocytopenic purpura et Preemptive rituximab prevents long-term relapses in immune-mediated thrombotic thrombocytopenic purpura).
Mis à jour le 13 Février 2022
Voir aussi :
- Mycophénolate mofétil [Fiche médicament]
- Immunoglobulines polyvalentes [Fiche médicament]
- Eculizumab [Fiche médicament]
- Rituximab en sous-cutané [Article]
Dernières actualités
- PTT congénital : La protéine ADAMTS13 recombinante bientôt disponible en accès précoce - publié le 26/03/24, [13147 clics]
- Essais thérapeutiques en cours - publié le 12/02/24, [12731 clics]
- Journée AD'venir 2023 - publié le 31/01/24, [11297 clics]
- Relabellisation du CNR-MAT - publié le 10/01/24, [43521 clics]
- Réunion du Centre de Référence 2023 - publié le 01/02/23, [14631 clics]









 La Clinique
La Clinique